二次性MRに対するMitraClipの患者選択
ボン大学ハートセンター 田中徹
今回は、COAPT trial とMITRA-FR trialとの違いに触れながら、二次性僧帽弁閉鎖不全症(MR)に対するMitraClip治療の患者選択についてまとめたいと思います。
【COAPT trial とMITRA-FR trial】
左室収縮能の低下を伴う二次性MRに対する経カテーテル治療であるMitraClipの有効性は2018年に発表されたCOAPT trial とMITRA-FR trialの2つのランダム化比較試験(RCT)で検討されています(1, 2)。
COAPT trialではMitraClipでの僧帽弁治療によって、薬物治療単独と比較してprimary endpointに設定されていた2年間の心不全再入院を有意に減少させることができました。加えて、secondary endpointの2年間の全死亡も減少させています。また、その効果は3年間の観察期間でも同様でした。一方で、主にフランスで行われたMITRA-FR trialでも、同様に薬物治療群とMitraClip群を比較されましたが、両群間で1年間の死亡・心不全入院率に有意な差は認められませんでした。上記のように同じ病態に対する同じ治療法を検討した、両RCTですが相反する結果となってしまいました。
この2つの試験がなぜ異なる結果になったのか、その理由は様々な側面から検討されています。簡単に両者の違いをまとめると下記の通りになります(3)。
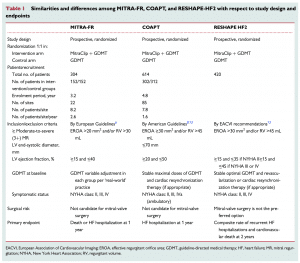
患者スクリーニングの厳密さや患者数、primary outcomeなどに加え、患者選択が異なります。COAPT trialではMITRA-FR trialよりもLVEFが高めの患者群で、かつ高度の左室拡大が除外されています。さらにMRの重症度もCOAPT trialでより高度に設定されていたことは注目されるべき点です。
【Proportionate/Disproportionate MR】
上記のようなCOAPTとMITRA-FRの両者の患者選択の違いから、二次性MRにおける左室拡大とMRの逆流量との関係性について注目されるようになりました。提唱されたのが下の図で表される”Proportionate/Disproportionate MR”という概念です(4)。MRの定量評価が左室拡大など左室のリモデリングに見合うっているものなのかどうか、という考え方です。
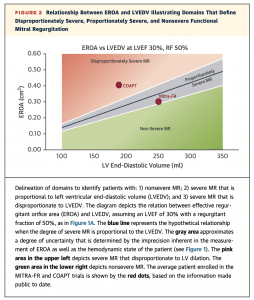
基本概念として、severe MRというのは”全心拍出の50%以上が左心房に逆流する状態“というのがコンセンサスとなっています(5, 6)。それに基づいて、定量評価であるEROA, Vena contractaなどのカットオフが定められています。そのように定義されているため、心拍出量によってsevere MRと診断されるために必要な逆流量が変わってくるということになります。したがって、左室拡張末期容積(LVEDV)と左室駆出率(LVEF)によって、severe MRと診断されるために必要な逆流量(i.e. EROA)が変化することになります。
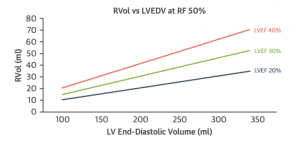
つまり、EROAが大きくてもそれ以上にLVEDVが大きければsevere MRとは言えない、ということで、それに基づいて提唱されたのがProportionate/Disproportionate MRという概念になります。2012年と2014年にそれぞれヨーロッパおよび米国のガイドラインにおいてsevere functional MRのEROAのカットオフが0.4 cm2 から0.2 cm2に引き下げられたのを受けて、MITRA-FR trial ではinclusion criteriaでEROA 0.2 cm2以上と設定されました。また、LVEFも低め(15-40%)に設定されたため、Proportionate/Disproportionate MRの考え方でいくと、non-severe MR (i.e. Proportionate MR)寄りになってしまいます。一方で、COAPT trialではEROA≧0.3 cm2とし、またLVEFも比較的高め(20-50%)、かつ高度の左室拡大の症例(LVDD≧70 mm)を除外したことにより、患者群はしっかりとsevere MR(i.e. Disproportionate MR)に相当しています。上記のような違いがあり、MRの治療の恩恵をCOAPT の患者群が最も受けやすかったのではないかと考えられています。
COAPT trialのpost-hoc analysisでも、MITRA-FR trialにentryしていたEROAが小さくLVEDVが大きい患者群(EROA≦0.3 cm2 かつLVEDV index≧96 ml/m2)ではMitraClip治療によって6分間歩行などの運動耐容能の改善は見られるものの、死亡・心不全入院の減少にはつながらなかったと報告されています(7)。
また、MITRA-FR trialではCOAPT trialと比較して、MitraClip後のMRの再発率も高かったことも指摘されています。severeのMRを再度認めた症例が、術直後でCOAPT trialの約2倍、1年後で約3倍認めていました。手技の修練度の問題もあるのかもしれませんが、左室拡大がMitraClipの手技成功率や術後のMR再発率と関連があることが報告されており、Proportionate/Disproportionate MRの概念が手技の成功率またdurabilityにも影響している可能性が考えられます(8, 9)。
【MITRA-FR trialでのProportionate/Disproportionate MRの検討】
そうなると、MITRA-FR trialの結果をProportionate/Disproportionate MRの考え方で説明ができるのか検証が必要になります。MITRA-FR trialの患者群におけるMRのProportionality の予後への影響を検討したpost-hoc analysisが、2021年にJACC imagingに報告されています(10)。
MITRA-FR trialの患者群を、MR重症度の定量評価項目(EROA, regurgitant volume, regurgitant fraction)と左室エコー指標(LVEF, LVEDV, LVESV, LVDD, LVSD, stroke volumeなど)、およびそれらの組み合わせでひたすらSub-group analysisでMitraClipの薬物治療に対する優位性を検討しています。COAPT trialが2年フォローまで達していたため、Endpointは24ヶ月の死亡・心不全入院とされています。
上図のCentral illustrationに結果がまとめられています。Proportionate/Disproportionate MRの図に合わせてみて、COAPTの患者群に近いところから遠いところまで多くのsub-groupで解析されましたが、いずれのサブグループでも交互作用は認められませんでした。Intention-to-treat analysisおよびper-protocol analysisのどちらも同様の結果でした。残念ながら、MITRA-FRの患者群でMRのProportionalityの有用性は示されませんでした。RCTといえどpost-hoc analysisであることと、いわゆるDisproporitonate MRにあたる患者数がかなりすくなくなってしまったので統計学的には少し無理のある解析であった可能性はあります。
【EROA/LVEDVという指標】
上記のような流れもあり、EROA/LVEDVというProportionate/Disproportionate MRの概念に基づく指標に注目が集まるようになりました。MITRA-FRのpost-hoc analysisではそのvalidationは明らかではありませんでしたが、real-worldのdataでその指標のMitraClip患者選択における有用性が検証されています。
EuroSMR registryというヨーロッパでMitraClipを施行された二次性MRのレジストリーデータからの報告で、2021年にJACC Imagingに掲載されています。
EROAおよびLVEDVが計測できている1,016名の患者(平均LVEF: 35.1±12.8%)をEROA/LVEDVの値によって3群に分類しています。
-MR-dominant (MD) group: EROA/LVEDV ≧0.165 cm2/per 100 ml
-MR-LV-co-dominant (MLCD) group: <0.165 and ≧0.115 cm2/per 100 ml
-LV-dominant (LD) group: <0.115 cm2/per 100 ml
それぞれのグループが上述のProportionalityのグラフにどのように当てはまるかは下図の通りです。
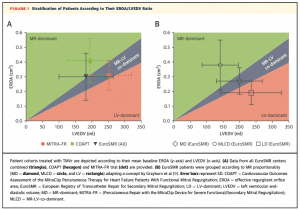
いずれの3群でもMitraClipにより十分なMR減少が得られており、NYHAの改善、6分間歩行距離の延長が得られました。しかし、有意差のあった患者背景で補正しても、LD群は他の2群と比較して、2年間の生存率は有意に低いという結果でした。
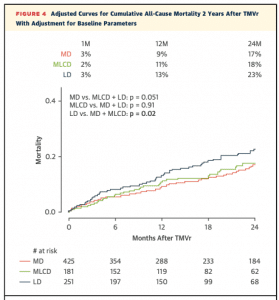
Proportionate MRに関してはカテーテルでのMR治療でも症状の緩和は得られますが、生存率の改善は十分には得られない可能性が示唆されます。EROA/LVEDVという指標は二次性MRの治療方針を決定する上で、今後さらに注目される指標かもしれません。
Proportionate/Disproportionate MRの考えがMitraClipを施行するかどうかの判断に有用なのかどうかはRCTで検討しなければ、確定的なことは言えません。
【COAPT criteriaという指標】
主なものとしてMRの重症度と左室容積という点に着目しましたが、患者選択という点においてCOAPT trial とMITRA-FR trialにはその他にも違いが見られます。EROA/LVEDVのように個別に評価を行うことも病態把握の点で非常に重要であると考えられますが、RCTの研究結果として考えるとCOAPT trialでの患者選択方法をそのまま臨床応用するのが、最も妥当と考えられます。実際に、2021年のESCガイドラインでも”COAPT criteria”としてEdge-to-edge カテーテル治療のdecision-makingに使用されています(11)。
そして、そういったCOAPT criteriaのreal-world での有用性についても検討されています。2021年にJACC Interventionに掲載されたイタリアやポルトガルなどの3施設からの報告です(12)。
MitraClipを施行した304名のLVEF低下(≦50%)を伴う二次性MRの患者において、2年および5年での全死亡、心血管死亡+心不全入院の発症率を調べています。患者は下図のCOAPT criteria (高度の左室拡大・収縮能低下、右心機能低下・高度の肺高血圧、不安定な血行動態)にしたがってCOAPT-like もしくはNon-COAPT-likeの2群に分けられています。結果、COAPT criteriaをすべて満たすCOAPT-likeの患者群はNon-COAPT-likeの患者群と比較して、患者背景で補正した上でも良好な予後を認めました。
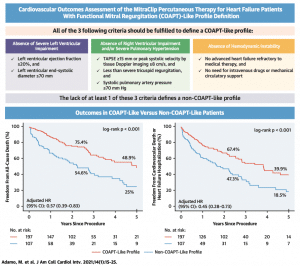
また、大きくわけると3項目になるCOAPT criteria (高度の左室不全、右心機能低下・高度の肺高血圧、不安定な血行動態)のうち、1つでも該当すると予後が悪化することも示され、特に右心機能低下・高度な肺高血圧、および不安定な血行動態が予後へ与えるインパクトが大きいことが認められました。
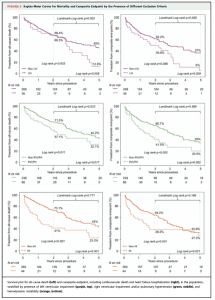
ESC2021で発表されたのみでまだ論文は未発表ですが、同じような検討は上述のEuroSMR registryのpopulationでも行われ、同様の結果が得られていました。また、MITRA-FR trialのpost-hoc analysisでもCOAPT criteriaの有用性についても検討されましたが、COAPT criteria該当群と非該当群で予後に有意差は認められませんでした(13)。しかし、RV functionのデータが欠落しているなど不十分なデータでした。これらを考慮すると、COAPT criteriaはMitraClip後の予後予測に有用であると考えられます。
【まとめ】
二次性MRに対するカテーテル治療の患者選択は非常に複雑だと思います。COAPT trial、MITRA-FR trialの2つのRCTの結果の違いを元に、エコー指標による僧帽弁カテーテル治療の患者選択について検討されています。EROA/LVEDVやCOAPT criteriaがMitraClip治療後の予後予測に有用であり、これらを元に患者選択を行うのが望ましいと考えられます。しかし、これらの条件を満たさない患者群でも症状の改善などの効果は得られており、治療の恩恵が全くないというわけではないと思います。
エコーパラメーター以外にもCOAPTとMITRA-FRの違いは指摘されており、その他の要素についても総合的に判断することが望ましいと考えられます。
【終わりに】
これで私のSUNRISE lab.でのレビューは最後になります。コロナ渦で紆余曲折もあり、だいぶ時間がかかってしまった上に、最後はかなり駆け足になりましたが、課題の10個のレビューも無事に終えることができました。内容としては、勉強不足の点もあったかと思いますが、こうしてまとめることで自分の知識の整理に加え、新たな研究テーマの発想にもつながりました。このような機会を与えていただいた中澤先生、重城先生、林田先生、藤堂様を始めとするSUNRISE lab.のメンバーの先生方には厚く御礼を申し上げます。
References
- Obadia JF, Messika-Zeitoun D, Leurent G, Iung B, Bonnet G, Piriou N, et al. Percutaneous Repair or Medical Treatment for Secondary Mitral Regurgitation. N Engl J Med. 2018;379(24):2297-306.
- Stone GW, Lindenfeld J, Abraham WT, Kar S, Lim DS, Mishell JM, et al. Transcatheter Mitral-Valve Repair in Patients with Heart Failure. N Engl J Med. 2018;379(24):2307-18.
- Pibarot P, Delgado V, Bax JJ. MITRA-FR vs. COAPT: lessons from two trials with diametrically opposed results. Eur Heart J Cardiovasc Imaging. 2019;20(6):620-4.
- Grayburn PA, Sannino A, Packer M. Proportionate and Disproportionate Functional Mitral Regurgitation: A New Conceptual Framework That Reconciles the Results of the MITRA-FR and COAPT Trials. JACC Cardiovasc Imaging. 2019;12(2):353-62.
- Dujardin KS, Enriquez-Sarano M, Bailey KR, Nishimura RA, Seward JB, Tajik AJ. Grading of mitral regurgitation by quantitative Doppler echocardiography: calibration by left ventricular angiography in routine clinical practice. Circulation. 1997;96(10):3409-15.
- Zoghbi WA, Adams D, Bonow RO, Enriquez-Sarano M, Foster E, Grayburn PA, et al. Recommendations for Noninvasive Evaluation of Native Valvular Regurgitation: A Report from the American Society of Echocardiography Developed in Collaboration with the Society for Cardiovascular Magnetic Resonance. J Am Soc Echocardiogr. 2017;30(4):303-71.
- Lindenfeld J, Abraham WT, Grayburn PA, Kar S, Asch FM, Lim DS, et al. Association of Effective Regurgitation Orifice Area to Left Ventricular End-Diastolic Volume Ratio With Transcatheter Mitral Valve Repair Outcomes: A Secondary Analysis of the COAPT Trial. JAMA Cardiol. 2021;6(4):427-36.
- Stolfo D, De Luca A, Morea G, Merlo M, Vitrella G, Caiffa T, et al. Predicting device failure after percutaneous repair of functional mitral regurgitation in advanced heart failure: Implications for patient selection. Int J Cardiol. 2018;257:182-7.
- Buck T, Eiswirth N, Farah A, Kahlert H, Patsalis PC, Kahlert P, et al. Recurrence of Functional Versus Organic Mitral Regurgitation After Transcatheter Mitral Valve Repair: Implications from Three-Dimensional Echocardiographic Analysis of Mitral Valve Geometry and Left Ventricular Dilation for a Point of No Return. J Am Soc Echocardiogr. 2021;34(7):744-56.
- Messika-Zeitoun D, Iung B, Armoiry X, Trochu JN, Donal E, Habib G, et al. Impact of Mitral Regurgitation Severity and Left Ventricular Remodeling on Outcome After MitraClip Implantation: Results From the Mitra-FR Trial. JACC Cardiovasc Imaging. 2021;14(4):742-52.
- Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2021.
- Adamo M, Fiorelli F, Melica B, D’Ortona R, Lupi L, Giannini C, et al. COAPT-Like Profile Predicts Long-Term Outcomes in Patients With Secondary Mitral Regurgitation Undergoing MitraClip Implantation. JACC Cardiovasc Interv. 2021;14(1):15-25.
- Iung B, Messika-Zeitoun D, Boutitie F, Trochu JN, Armoiry X, Maucort-Boulch D, et al. Characteristics and Outcome of COAPT-Eligible Patients in the MITRA-FR Trial. Circulation. 2020;142(25):2482-4.
