TAVR の前にPCI?
ボン大学ハートセンター リサーチフェロー 田中徹
今回は、冠動脈病変を合併した大動脈弁狭窄症(AS)患者に関するランダム化比較試験であるACTIVATION trialの結果についてまとめます。ACTIVATION trialは冠動脈狭窄を合併したsevere ASに対し、大動脈弁カテーテル治療(TAVR)の術前にPCIを行うことの妥当性について検討したランダム化比較試験で、試験の結果自体は2020年のPCR valvesにて発表されていたものです。論文は2021年のJACC interventionに掲載されました(1)。
【Background】
冠動脈疾患はASに多く合併する併存疾患の一つで、およそ半数から2/3程度の症例に認められることが知られています。また、そうした冠動脈病変はTAVR後の予後不良因子のうちの一つであり、どのように血行再建を行うかが臨床上で問題になります。
TAVR患者におけるPCI施行のタイミングに関しては、これまでいくつかの観察研究の報告があります。TAVRの術前、術後、もしくは同時にPCIを施行してもハードエンドポイントには大きな差が見られず(2)、術前のPCIはAKIなどの合併症や出血性イベントのリスクが上昇する可能性が指摘されています(3)。しかし、これまでRCTでの検討はされておらず、ACTIVATION trialはTAVR術前のPCI施行について、PCI非施行に対する非劣性を証明するために組まれたRCTになります。
【Methods】
ACTIVATION trialはprospective, randomized, open-label trialで、UK、フランス、ドイツの17施設が参加しています。
Inclusion criteria
・TAVRが施行可能なsevere AS
・少なくとも1病変以上の冠動脈狭窄病変 (70%以上の狭窄)
-各Operatorが冠動脈造影をもとに判断
-Protectedの左主幹部病変や静脈グラフト病変は50%以上の狭窄
-冠動脈分枝部病変は除く
Exclusion criteria
・Enrollment前30日以内のACS
・高度の狭心症状 (CCS angina class III or more)
・Unprotectedの左主幹部病変
・DAPT禁忌症例
上記を満たす患者をTAVR前にPCI施行する群と非施行群に1:1でランダム割付しています。PCIの手技自体や手技後のDAPT期間などはoperatorに委ねられており、PCI で用いるstentもBoston Scientific のものであればベアメタルステントか薬剤溶出性ステントでも使用可能なプロトコールとなっていました。TAVRに関しても治療ストラテジーや使用する人工弁もoperatorの判断に委ねられています。
サンプルサイズは過去の報告から推測されるイベント発症率を参照に、90%の検出力、年間5%のロストフォローを加味して、310名が予定されました。
Primary endpoint: TAVR手技から1年以内の複合エンドポイント (全死亡、再入院)
-TAVRが施行されなかった症例ではPCI時、もしくはランダム化から1年の期間で評価されています
-非劣性マージンを7.5%に設定
Secondary endpoint: ランダム化から1年以内の死亡、出血イベント、MACCE (死亡、心筋梗塞、AKI)
【Results】
2012年12月から2019年1月にかけて合計235名がenrollmentされました。当初は310名の参加が予定されていましたが、2017年以降enrollmentが進まず、早期に中断となっています。Patient flowchartは下記の通りです。
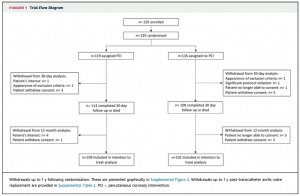
235名のうち、119名がPCI施行群、116名がPCI非施行群に割り付けされています。全体の平均年齢は84歳程度で、STS-PROM も4.4%前後と、高齢の中等度リスクのTAVI患者群といったpopulationです。
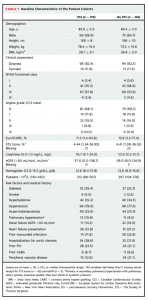
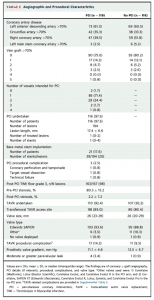
PCI施行群に割付された患者のうち、97.5%で実際にPCIが施行され、その多くが1病変のみの治療で完了しています。また、およそ18%の患者でベアメタルステントを用いて治療が行われています。PCI自体の合併症の頻度は2.5%という結果で、比較的安全に施行できていたと考えられます。
両群それぞれで92%、94%の患者でTAVRが施行され、多くでSapien 弁が使用されています。PCI非施行群ではfemoral approachの頻度が少ない傾向にありました。ランダム化からTAVR施行までの期間はPCI施行群で中央値41日、PCI非施行群で中央値27日であり、PCIを施行することでおよそ2週間程度のdelayが生じたようです。
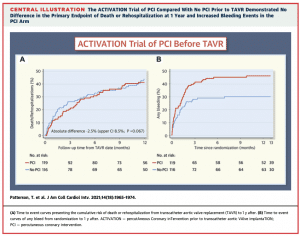
Intention-to-treat populationにおいて、Primary endpointである1年以内の全死亡・再入院率はPCI施行群で41.5%, PCI非施行群で44.0%であり (Figure 2A)、1-sided upper 95% confidence limit は8.5%でnon-inferiority test p-value =0.067とTAVR術前のPCI施行群の非劣勢は示せない結果でした。As-treated populationでも、primary endpointに関しては同様の結果で非劣勢を示せていません(1-sided upper 95% confidence limit: 7.5%; p for noninferiority =0.050)。
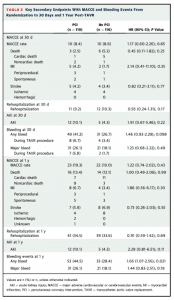
Secondary endpointの結果として、MACCEはPCI施行群で高い傾向にあり(HR 1.22; 95%CI: 0.74-2.02)、また、全出血イベントに関してもPCI施行群で有意に高いという結果でした(HR: 1.66; 95%CI: 1.07-2.56)。Major bleeding やAKIなどの頻度も有意差はないもののPCI施行群で高い傾向にありました。
抗血小板・抗凝固療法に関してもデータが記載されおり、簡単に下表にまとめました。PCI施行群の方がDAPT使用率は全観察期間にわたって高い傾向にありましたが、抗凝固療法自体の使用率は両群間で同程度でした。
| PCI施行群 | PCI非施行群 | ||
| TAVR退院時 | DAPT | 62.9% | 31.0% |
| SAPT+warfarin | 10.1% | 11.2% | |
| DAPT+warfarin | 7.6% | 2.6% | |
| TAVR 30日後 | DAPT | 49.6% | 24.1% |
| SAPT+warfarin | 19.3% | 17.2% | |
| DAPT+warfarin | 6.7% | 1.7% | |
| TAVR 1年後 | DAPT | 9.2% | 4.3% |
| SAPT+warfarin | 13.4% | 4.3% | |
| DAPT+warfarin | 0.8% | 1.7% |
【結論】
冠動脈狭窄を有するsevere ASの症例でTAVR術前のPCI施行群はPCI施行群と比較して、TAVR後1年の死亡・再入院のイベント率は同程度でしたが、非劣性マージンを満たせず、非劣性を証明できませんでした。
MACCEの頻度はPCI施行群と非施行群で同程度でしたが、全出血イベントはPCI施行群で多く、そのほとんどがTAVR後30日以内に発症しており、PCI後のDAPTがその原因であった可能性が指摘されています。
【まとめ】
実臨床で多く目にする冠動脈病変を有するTAVR患者のPCI施行に関するRCTでした。2011年に立案され2012年から開始された本研究であり、その段階でこのようなクリニカルクエスチョンにアプローチしていたことに感心します。しかし、研究としてenrollmentが思うように進まず、途中で打ち切りとなってしまいました。その原因としては、術前CTを施行して冠動脈造影を施行せずに直接TAVRを行う症例が増えたことが挙げられています。そのような背景もあってか、本試験で検討を試みていたTAVR術前のPCI施行の非劣性は証明できませんでした。
私見としては、本研究においてなぜPCI施行群の非劣性を証明しようとしたのかはやや疑問です。安全性やコストなどを考えれば、PCIを施行しないことの非劣性を証明すること(PCIしなくても安全ということ)の方が臨床的意義は高いように思いました。
また、本研究結果を実臨床に応用できるのはやや限定的なように思います。まず、試験実施期間が2012年から2019年と長期間になっていることが、このtrialの問題であるとも考えられます。その間、TAVRのデバイスや手技は確実に進歩し、また、PCIのステントや術後のDAPT療法にも多くの知見が得られました。特にDAPT期間の短縮や抗凝固療法の併用期間など、出血性イベントを減らすための知見が多く出てきており、それらが本研究結果に十分反映できているかはわかりません。臨床に応用するのにはやや限定的になってしまうかもしれません。さらに、冠動脈病変に関しても、冠動脈造影のvisualでの狭窄で治療適応を判断しており、physiological な評価が欠けていたことも一つの問題です。また、治療もベアメタルステントをおよそ20%程度で使用するなど、現在のスタンダードからは少しずれている印象を受けました。
結果として、これまでの観察研究で指摘されていたTAVR術前のPCI施行がAKIや出血などのイベントの増多につながることが改めてRCTでも示され、ASの術前にPCIを施行する妥当性は低くなったと思います。また、TAVR後の冠動脈アクセスを考慮したTAVR弁の留置方法についても知見が深まっており、TAVR後のPCIをそこまで避ける必要性も少なくなっているように感じます。よほどの冠動脈狭窄や強い狭心症状、主幹部病変などがなければ、ASの解除後にPCIを施行するのが妥当なのかもしれません。
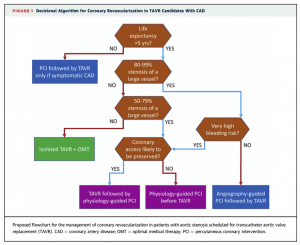
この論文に対するEditorialではACTIVATION trialの結果も考慮して、下記のようなdecision makingが提案されていました(4)。患者予後、出血リスク、病変の重症度に加え、TAVR後の冠動脈アクセスを考慮しつつ、PCIのタイミングを判断することが提唱されており、Reasonableなフローチャートだと思います。
References
- Patterson T, Clayton T, Dodd M, Khawaja Z, Morice MC, Wilson K, et al. ACTIVATION (PercutAneous Coronary inTervention prIor to transcatheter aortic VAlve implantaTION): A Randomized Clinical Trial. JACC Cardiovasc Interv. 2021;14(18):1965-74.
- Ochiai T, Yoon SH, Flint N, Sharma R, Chakravarty T, Kaewkes D, et al. Timing and Outcomes of Percutaneous Coronary Intervention in Patients Who Underwent Transcatheter Aortic Valve Implantation. Am J Cardiol. 2020;125(9):1361-8.
- Venturi G, Pighi M, Lunardi M, Mainardi A, Del Sole PA, Tavella D, et al. Contrast-Induced Nephropathy in Patients Undergoing Staged Versus Concomitant Transcatheter Aortic Valve Implantation and Coronary Procedures. J Am Heart Assoc. 2021;10(15):e020599.
- Petronio AS, De Carlo M. To Revascularize or Not to Revascularize TAVR Candidates?: That Is the (Lingering) Question. JACC Cardiovasc Interv. 2021;14(18):1975-7.
