IVUS-XPL Study 5年の結果、Intracoronary Imagingのエビデンス
論文レビュー第三弾
みなさんこんにちは、CRFの清家です。
今回はIVUS-XPL 5年の成績
Hong SJ, et al. Effect of Intravascular Ultrasound-Guided Drug-Eluting Stent Implantation: 5-Year Follow-Up of the IVUS-XPL Randomized Trial. JACC Cardiovasc Interv. 2020;13:62-71.
の論文のレビューをさせていただきたいと思います。
まずその前に、Intracoronary Imaging Labに留学している身として、Intracoronary Imagingの医学的効果、経済的効果のエビデンスをサマライズしていきたいと思います。
日本という特殊な環境:
ご存じの方も多いと思いますが、IVUS/OCTが当たり前のように日常臨床で使われている国は日本だけです。
一般的に、日本ではIVUS/OCTは95%程度、米国では20%程度、ヨーロッパでは10%程度のPCIで使用されていると言われています。実際には、特にヨーロッパでは研究関連で使用されることが多く、実臨床での使用率はさらに低いと言われます。
まず、IVUS/OCTの使用による予後への効果を見ていきたいと思います。
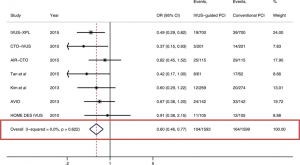
(1)ご覧いただいた通り、IVUSの使用ではMACEが0.6まで低下するとされています。そのほかのMeta-analysisをまとめたものがreview articleでまとめられていますが、下記のようにやはりどのMeta-analysisでもMACEは6割程度まで減少しています。
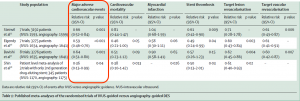
ここで問題となるのが、経済的な負担、効果です。
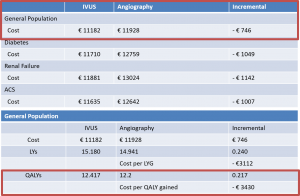
Alberti A, Giudice P, Gelera A, et al. Understanding the economic impact of intravascular ultrasound (IVUS). Eur J Health Econ. 2016; 17: 185–93.
このペーパーでは、1患者当たりの治療費がIVUSの使用で合併症などを減らすことにより745€減少させると報告しています。さらに、1 QALY*を得るために-3,430€の費用が必要であると報告しています。必要な金額がマイナスですので、予後を改善しつつ医療費を減少させるということになります。
* 質調整生存年(しつちょうせいせいぞんねん, Quality-adjusted life year, QALY): 費用対効果分析でよく用いられる指標で、生存における量と質の2点を評価する手法です。1 QALYは、完全に健康な1年間に相当します。
従って、まとめるとIVUS/OCTの使用によりMACEが40%程度減少し、かつ医療費も抑制されると報告されています。
IVUSに関する無作為化対照試験は、私の調べた限り9個あり、現在までで最大の試験がIVUS-XPL試験となります。
IVUS使用後の長期成績となり、その結果が注目されていました。
5年目の結果を見る前に、IVUS-XPL1年目の結果を見てみたいと思います。
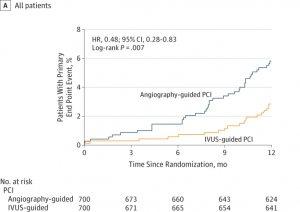
ご覧いただいた通り、HR 0.48という結果であり、1年間の間におおよそ半分MACEを減らすと報告されていました。
それでは、論文の内容に入っていきたいと思います。
【Introduction】
IVUS-XPL試験において、IVUSの使用により1年予後の有用性が報告された。しかし、5年予後に関しては知られていない。今回の研究の目的は、長期間にわたってその有益性が持続されるかを検討することです。
【Methods】
病変長の長い病変に28 mm以上のXienceステントを留置する1,400症例が対象とされた医師主導の多施設共同無作為化試験です。Angio-Guide群 (n=700)、IVUS-Guide群 (n=700) に割り当てられました。
Primary endpointは、MACE (心臓死、標的病変心筋梗塞、虚血による標的病変血行再建の複合エンドポイント)とされました。
【Results】
平均年齢は63歳で、EAPとACSが約半数ずつエントリーされています。
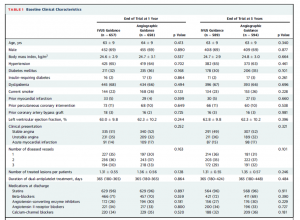
手技背景ですが、
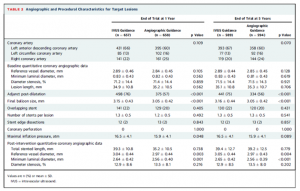
Enrollが28 mm以上のステントが必要な症例となっているために、平均ステント長が39 mm程度のlong stentingがなされております。また、ステント留置後に後拡張された率がIVUS群で有意に高く、有意にBalloon sizeが大きいという結果でした。
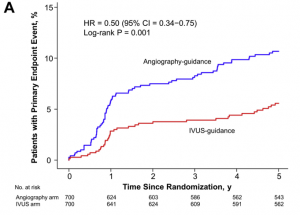
そして、1-5年のHRは0.5 (95% CI: 0.34 to 0.75; p=0.001)であり、治療後5年までIVUSの有益性は持続しました。
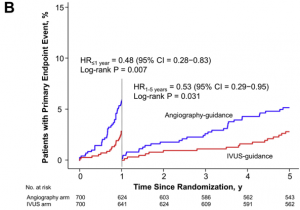
さらに、1年を基準としたLandmark解析においてもHR 0.53 (95% CI: 0.29 to 0.95; p=0.031)と有益性が認められました。

Subgroup解析においても、基本的にはどのような群においてもIVUS-Guideが有効であると考えられた。
【Discussion】
Angio-guidanceと比較し、IVUS-guidanceでは5年間その有益性は継続し、おおよそ半分のMACEを減少させており、1年以後もその効果が証明されたと結論付けられています。
これまでのRandomized研究では2年目までの予後のみのであったが、本研究では5年後までの効果が証明されました。
また、IVUS群に割り振られた症例で、最終的なIVUSのクライテリアを満たせなかった症例に関しては予後が悪かったことは特筆すべき点です。今回使用されたIVUS クライテリアは、MSA (ステント内の最小内腔面積)がDistal referenceのRLA (遠位部の内腔面積)より大きい事としています。IVUSクライテリアをを満たせないような病変が悪いのか、それともIVUS クライテリアを満たせなかった事が悪いのかというのは難しいところですが、いずれにせよ、やはり最低限Distal RLAよりステントを拡張することを目標にPCIを行うことは重要であると思われます。
【私見】
ESCのガイドラインでは2018年の改定において、IVUS/OCT guide PCIがClass IIb→IIaに繰り上げされました。ACC/AHA/SCAIのガイドラインではClass IIbです。しかし、現在欧米においてIVUS/OCTの使用が全体的に増加しているということはないようです。
また、このようなランダマイズ研究に登録するような施設ではIVUSの読み方、またIVUSを通過させる技術などのLearning curveはすでに超えていると思いますが、今までIVUSを使用してこなかった施設では、IVUSのメリットは低下すると思われます。
世界にIVUS/OCT-Guide PCIが普及するのはいつになるのでしょうか?
ISCHEMIA試験でもState-of-the Art PCIがされていない事が、PCI群の予後があまり改善しなかった要因の一つと考えられます**。
PCIのIndicationや効果についての議論が多いですが、その前にImagingの使用によりPCI早期の合併症をしっかりと減らすことが前提と感じています。
** 個人的な感想を書かせていただきます。ISCHEMIA試験では術後のHigh sense Troponinの上昇もMIと定義し、Spontaneous MIと同一のものとしてPrimary endpointに入れるという統計解析がされています(下記参照)(5)。日本で行われたSTOP-DAPT II試験(6)では、TroponinはToo sensitive (本文まま: because the evaluation by troponin is too sensitive.)ということでCK-MBを用いてPeri-procedural MIが決定されています。いわゆる一般的な心筋梗塞Spontaneous MIと、術直後のTrop Pの上昇を同等のイベントとして判断することは、やや無理があると感じます。そして、ISCHEMIA試験ではSpontaneous MIはPCI群にて有意に低下(HR 0.67, P<0.01)しています。
論文はどうしても、Primary endpointの結果が一人歩きしてしまいます。このように社会にインパクトのある論文はどのような基準のPrimary endpointが使用されているのか、我々はしっかりと判断していく必要があると思います。

References
(1) Elgendy IY, et al. Circ Cardiovasc Interv. 2016;9:e00700
(2) Mintz GS, Gualiumi G. Lancet. 2017;390:793
(3) Alberti A, Giudice P, Gelera A, et al. Eur J Health Econ 2016; 17: 185–93.
(4) Maron DJ, et al. Am Heart J. 2018 Jul;201:124-135.
(5) Maron DJ, et al. Am Heart J. 2018;201:124-135
(6) Watanabe H, et al. JAMA. 2019;321:2414-2427.
