非虚血性心不全症例におけるMRI: OUTSMART-HF trial
今回は久々にMRIに関しての論文です。MRIは一度の検査で心機能、冠動脈評価、心筋障害評価など、大変多くの情報量を得ることができ、時間分解能、空間分解能も高く、非常にpowerfulなimaging toolですが、本論文は果たして非虚血性の心不全に対するroutineでの使用の有用性はどうなのか?という点に踏み込んだRandomized trialです。
[1] Paterson DI, et al. OUTSMART HF: A Randomized Controlled Trial of Routine Versus Selective Cardiac Magnetic Resonance for Patients with Non-Ischemic Heart Failure (IMAGE-HF 1B). Circulation. 2020;10.1161/CIRCULATIONAHA.119.043964.
若干用語がわかりづらいのですが、infiltrative = サルコイドーシス、アミロイドーシスなど、inflammatory = 心筋炎など、specific HF etiology = 診断により特定の治療を選択できる疾患群、といった理解で良いかと思います。
[背景]
非虚血性心不全は心不全の原因として先進国の約50%以上、発展途上国の60%を占めており、心室の拡大、肥大、炎症などを伴う心筋症を背景とすることが多い。様々な心筋症においてその原因に特異的な治療が行われるため、その鑑別は非常に重要である。心エコーは最も一般的な検査であるが、心筋症の原因の鑑別は困難である。
心臓MRI(以下CMR)は高い再現性を持ち、心臓の構造と機能の評価と心筋組織診断が可能であり、非虚血性心不全診療において魅力的な検査である。非造影のT1, T2画像は心筋繊維化や浮腫を判別することができ、LGE画像のパターンは様々な心筋症の有用な所見を得ることができる。あるレジストリーデータでは心筋炎/心筋症についての精査のためにCMRは頻繁に利用されており、11%の症例で新たな診断が得られ、55%で治療に影響を与えたことが報告されている[2] 。現在のガイドラインでは心不全が疑われるもしくは心不全と診断された症例の精査にCMRを推奨しているものの、その根拠となるエビデンスのレベルは高くない。また、コストと汎用性の面からCMRの使用は限られている。しかし、現時点で心不全に対するMRIの臨床的有用性を示した大規模randomized trialはない。
そのため、本研究では非虚血性心不全に対するルーチンでのCMR使用が選択的なCMR使用と比較し診断率が向上すると仮定し研究を行なった。
[方法]
デザイン: 詳しいトライアルデザインは文献[3]に示してあります。全部は詳しく述べられないので、以下要約です。
Inclusion criteriaは18歳以上の新規もしくは悪化を認め、臨床的に非虚血性心筋症もしくはHFpEFと診断されたNYHA 2度以上の症例であり、インフォームドコンセントを取得後Routine CMR群とSelective CMR群に1:1に無作為に割り付けられた。Selective CMR症例におけるCMRはプロトコル上、infiltrative cardiomyopathy、ARVC、adult congenital heart disease, pericardial diseaseが疑われた場合に使用が推奨された。
カナダの10施設、フィンランドの3施設において12ヶ月以内に心不全と診断された、もしくは心不全の診断がついており12ヶ月以内に悪化を認めた連続症例がスクリーニングされた。
以前にCMRが撮影されている症例で臨床的変化がない、すでに心不全の原因が特定されている、虚血性心疾患が証明されている、心不全に対する集中治療が継続的に必要である、手術が予想される弁膜症を有する、CMRやガドリニウムに対する禁忌がある、予後が3ヶ月以内と予測されている、などの症例は除外された。
Figure 1は試験のデザイン。被験者は試験への登録時、画像検査時、1ヶ月後、3ヶ月後の4点で評価され、それぞれの時点でHF etiologyの判断が担当医によって行われた。Baseline時点で、HF etiologyは担当医により次のカテゴリーより最も疑わしいものに分類された(idiopathic dilated、HFpEF、inflammatory、infiltrative、hypertrophic、ischemic、valvular、mixed、other, unknown)。
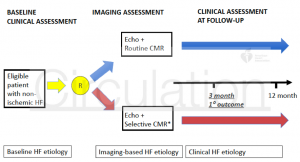 (Figure 1)
(Figure 1)
画像評価: TTE, CMRの方法は割愛します。画像診断医によりecho, CMRのそれぞれについて前述のカテゴリーに基づき心筋症の分類が行われた。CMRを行なった群ではCMRでの診断がechoの診断に優先された。画像診断医はblindでの診断を行なった。一方、担当医は試験デザイン上blind不可能であったため、open-labelでCMRでの介入の要否を判断した。
アウトカム: Primary outcomeは3ヶ月時点でのCMR, echoを含む全ての臨床情報に基づいた担当医の治療可能な心不全の診断(specific HF etiology)とされた。特定の治療可能なetiologyはinflammatory, infiltrative, hypertrophic, valuvular, mixed, otherのカテゴリーが定義された。一方でdilated、HFpEF、unknownは特定の治療のないetiology (non-specific etiology)と定義された。
Secondary outcomeとして、ルーチンでのCMR使用が予後に及ぼす影響を調査した。3ヶ月、12ヶ月時点で全死亡、心臓血管関連の入院が調査され、さらに心不全に対する薬物治療、デバイス植え込み、電気生理学的検査施行、心臓手術もしくは移植、疾患特異的な心不全治療の有無についても調査された。
[結果]
2011年1月から2016年10月まで、518人の非虚血性心不全患者が選択されRoutine CMR群とselective CMR群にランダム化された。(Figure 2)
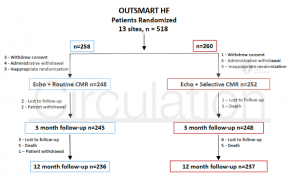 (Figure 2)
(Figure 2)
除外された患者を除き、計500例(平均59±13歳、男性 69%)がITT解析に用いられた。Routine CMR群248例、Selective CMR群252例のbaseline dataはTable 1に示されており、特に差はない。両群とも37%がspecific HF etiologyに分類され、心不全の予後リスク層別化に用いられるMAGGIC risk scoreは両群共19±6であった。
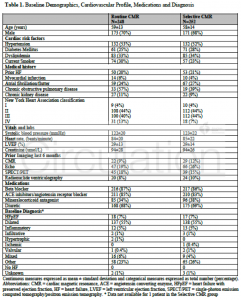 (Table 1)
(Table 1)
Primary outcomeについて: 3ヶ月時点では両群についてprimary outcomeに有意な差はなく(p = 0.22)、selective CMR群では44%, CMR群では50%でspecific HF etiologyが診断された。(Table 2)
 (Table 2)
(Table 2)
12ヶ月時点でのintention-to-treat (ITT)解析でも同様の結果であった。ベースラインでの診断と比較し、Routine CMR群で3ヶ月時点での新たなHF etiologyの診断は18% (45/245)であり、selective CMR群では22% (55/248)であり、有意差を認めなかった (p=0.29)。Primary outcome (specific HF etiologyの診断)に関しての多変量解析では、baselineでのHF etiologyの診断が独立したspecific HF etiologyの予測因子だった。(Table 3)
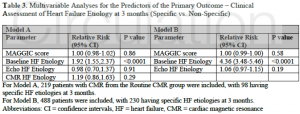 (Table 3)
(Table 3)
画像診断結果に関して: Routine CMR群では248例中224例(90%)でCMRが施行された。24例では閉所恐怖症もしくは担当医の判断でCMRが施行されなかった。一方selective CMR群では251例中61例 (24%)でCMRが施行されたが、プロトコルでの推奨通りに行われたCMRは3/61例のみであった。Routine CMR群では34%, selective CMR群では30%でSpecific HF etiologyの診断がなされた (p = 0.34) (Table 4)。
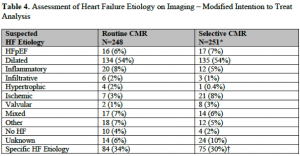 (Table 4)
(Table 4)
Routine CMR群における解析では、CMRによるspecific HF etiologyの診断率は36%, echoによる診断率は20%であった(p < 0.001)。(Table 5)
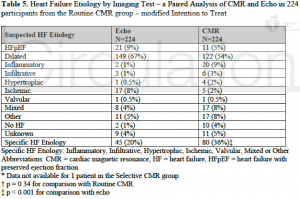 (Table 5)
(Table 5)
予後について: Routine CMR群とselective CMR群で12ヶ月後のevent-free survivalに有意さを認めなかった(Figure 3)。また、患者の臨床経過や薬物治療、侵襲的治療などに関しても差を認めなかった。
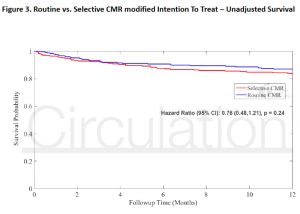 (Figure 3)
(Figure 3)
画像診断によるSpecific HF etiologyの診断を受けた患者群は、non-specificであった患者群と比較してイベントが多く認められた (19% vs. 12%, p = 0.02) (Figure 4a)。一方で3ヶ月時点での担当医による臨床的判断によるspecific HF etiologyの診断はnon-specificであった群と比較し12ヶ月時点のevent rateに有意差を認めなかった(15% vs. 14%, p = 0.49) (Figure 4b)。
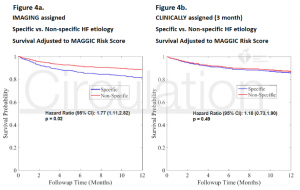 (Figure 4a, 4b)
(Figure 4a, 4b)
[考察]
本研究は、非虚血性心筋症に対してCMRを画像診断にどのように組み込むかについてのmulticenter randomized trialである。結果として、今回の対象患者においてroutineでのCMR使用はselectiveな仕様と比較してspecific HF etiologyの診断率を向上させなかった。一方でエコーのみと比較し、CMRはspecific HF etiologyの診断率を向上させ、画像診断によるspecific HF etiologyの診断は臨床的診断よりも予後が悪いことが示された。
Routine CMRがspecific HF etiology診断率を向上させなかった理由として、selective CMR群のうち24%もの患者がプロトコルにないCMRを行なっていたことが挙げられる。
Secondary analysisでは、CMRがechoと比較しspecific HF etiologyの診断において16%の向上を認めていた。しかしSpecific HF etiologyの診断は予後が悪いにも関わらず、Routine CMR群での予後の改善効果は認められず、その後の治療に関しても特に変化は見られなかった。この結果はCMRの結果、specific HF etiologyの診断がrisk評価に重要であるにも関わらず臨床判断に反映されていない可能性を示唆していると考えられた。
[結論] 非虚血性心不全の診断について、CMRのroutineでの使用はselectiveな使用と比較し診断の向上は得られず、予後にも差はなかった。Secondary analysisではCMRはechoに比較し心不全原因の特定に有用であり、画像診断により特定の診断が得られたの予後は悪かったものの、臨床的な診断に反映されていなかった。
[私見] 今回の論文は流石にCMRを非虚血性心不全全例で行うのは大変だな…という臨床医の気持ちが反映されたかのような結果でした。RoutineでのCMRの使用についてはnegativeな結果となりました。CMRで500例近いデータはかなり魅力的ですが、今回の論文はCMR自体の画像評価というよりはCMRによって導き出された診断についてなのであまり個々の診断の詳細について記載はありませんでした。
残念だった点の一つとしては、筆者らもlimitationに記載している通り、selective CMR群でprotocolに沿わないCMR施行例が24%もいたこと。せっかくrandomized control trialなのに、これによりかなり検出力が低下してしまっています(かといって差はつかなかったと思いますが)。 また、secondary outcomeに関しては画像診断のみで予後を改善するというのはなかなかハードルが高かったような気がします。研究デザインに関してはもう少し改善の余地があったのではないかというのが正直な感想です。
もう一点は、画像による診断と臨床診断のズレが大きかったこと。そしてその原因までは調査されていないことです。おそらく臨床経過などからなのでしょうが、意外とCMR撮ってもその所見を採用しないことも多かったようです。CMRの診断が確立され、信頼性が向上している今であれば違った結果になるかも…少しこのtrialを行う時期が早すぎたのかもしれません。
最後に、エコーとの比較について。エコーは各施設の標準的な撮像基準に委ねられているので、advancedな評価については不明です。特にアミロイドーシスなどはストレインエコーなどにより診断が向上する可能性などもありますので、単純に結論として『エコーよりCMRの方が診断率が高かった』と言えるのかは疑問です(CMRも標準的なプロトコルでしか行われていないので、逆もまた然り)。
私はrandomized control trialを解析したことはありませんし、デザインしたこともないのですが、私見開始時のデザイン設定の難しさなどを感じた論文でした。
ひとまず今の所はまだCMRがRoutineで行われる時代ではないようです。10年経ったら結果は変わっているかもしれません。
[1] Paterson DI, et al. OUTSMART HF: A Randomized Controlled Trial of Routine Versus Selective Cardiac Magnetic Resonance for Patients with Non-Ischemic Heart Failure (IMAGE-HF 1B). Circulation 2020, doi: 10.1161/CIRCULATIONAHA.119.043964. Epub ahead of print.
[2] Bruder O et al. EuroCMR (European Cardiovascular Magnetic Resonance) registry: results of the German pilot phase. J Am Coll Cardiol 2009;54:1457-1466.
[3] Paterson DI, et al. Routine versus selective cardiac magnetic resonance in non-ischemic heart failure – OUTSMART-HF: study protocol for a randomized controlled trial (IMAGE-HF (heart failure) project 1-B). Trials 2013;14:332.
