二次性MRに対する至適な薬物治療とは?
ボン大学ハートセンター 田中徹
今回は二次性僧帽弁閉鎖不全症(MR)への至適薬物治療についてまとめます。
僧帽弁自体に器質的障害のない二次性MR、特に左室拡大や収縮障害による心室性二次性MRに対する治療方針は近年で大きく変化しました。2018年にCOAPT trialが発表され(1)、MRに対するカテーテル治療であるMitraClipが薬物治療群に対して、死亡・心不全入院の抑制効果を示しました。このCOAPT trialの結果をもって、日本および欧米のガイドラインではLVEFが20-50%と低下に伴う二次性MRに対してMitraClipでの治療を推奨するようになりました。そして、2021年に改定されたESCのガイドラインではCOAPT criteria (*注)を満たしていれば、Class IIaとして推奨されています(2)。とはいっても、あくまでも“薬物治療を最大限行った上での”という但し書きがついての推奨であり、“二次性MRに対する治療の第一選択は薬物治療である”という点はゆるぎありません。心不全のガイドラインに準拠して、必要な心不全薬を可能な限り増量した上で、MitraClipの適応を検討することが求められています。
* COAPT criteria: COAPT trial のInclusion and Exclusion criteria。LVEF 20-50%, LV end-diastolic diameter ≦70mmなど。
そのような二次性MRをもつ心不全患者に対する薬物治療の目的は主に以下の2点になるかと思います。
- 左室収縮障害を呈する心不全としての予後の改善
- 左室リバースリモデリングを介してMRの減少
【1. 薬物治療による予後改善効果】
まず、心室性二次性MRは左室の拡大や収縮障害によって生じるものであり、そうした二次性MRが生じてしまうほど左室拡大や収縮障害が高度であるとも考えられます。そのため、それらの収縮障害を伴う心不全として(MRはおいておいて)、左室のリバースリモデリングや予後改善を期待し、一般的な心不全治療薬の投与が必要と考えられます。
また、LVEFの低下を伴う二次性MR患者にフォーカスした観察研究でも、ガイドラインに準拠した薬物治療(Beta-blockers+RAAS inhibitors+MRAs)を十分に導入できていないことが予後不良因子であることが報告されています(3)。
今回のESCの心不全ガイドラインの改定に伴って、LVEF40%以下ではこれまで推奨されていたBeta-blockers, RAAS inhibitors, MRAsに加え、ARNIやSGLT2 inhibitorsも新たに追加されており、それらを組み合わせて治療を行っていくのが望ましいと考えられます。一方で、今回LVEF 40-50%の”Mildly reduced EF”の患者群に対する薬物治療も初めてガイドラインに記載されたので、COAPT trialにも含まれていたこのカテゴリーの患者群もガイドラインを参照して薬物治療を調整することが必要です。
【2. 薬物治療によるMR減少効果】
もう一点は、薬物治療でMRの減少を目指すことも可能です。薬物治療で減少するのであれば、カテーテル治療を回避することができ、不必要な手技をなくすことができます。現時点で二次性MRの減少に効果が報告されている薬剤はBeta-blockers, ACE inhibitors, ARB, ARNIです。その一部を下記まとめます。
・Beta-Blockers
かなり古い研究になりますが、beta-blockerの左室収縮障害を伴う心不全患者に対するRCTで、二次性MRの変化も評価されています(4, 5)。MetoprololやCarvedilolといった薬物治療の導入によって左室リバースリモデリングと同時に二次性MRを減少させたことが報告されています。
・ACE inhibitors
これもかなり前ですが、1998年にLisinoprilの二次性MR患者における有用性が観察研究にて検討されています(6)。LVEF低下を伴うModerate-to-severe 以上の二次性MR患者に、高用量のLisinopril+Isosorbide dinitrateを開始し、およそ40%でMRが中等度以下まで改善が得られています。
・ARNI
最近話題のARNIに関しては、2019年に二次性MR患者に対するsacubitril/valsartanのRCTであるPRIME trialが報告されています(7)。LVEF 25-50%の二次性MR患者で、beta-blockersとACE inhibitorを6ヶ月以上使用していてもMRが残存(EROA >0.1cm2)している118名をsacubitril/valsartan群、valsartan群に1:1割付しています。それぞれの薬剤は可能な限り最大用量まで増量を行うこととされています。Primary endpointは12ヶ月後のEROAに設定されていました。12ヶ月後にフォローアップできたsacubitril/valsartan群 (51名),valsartan群 (53名)が解析され、EROAはsacubitril/valsartan群でより減少幅が大きかった(-0.058±0.095 cm2 vs. -0.018±0.105 cm2, p=0.032)という結果でした。一方で、死亡や心不全などのアウトカムに関しては両群間で差はみられませんでした。両群共にsacubitril/valsartanもしくはvalsartanの12ヶ月時点での継続率は100%と良好な服薬アドヒアランスで、十分な用量まで増量ができていました。
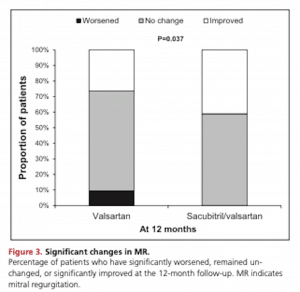
結果としては、ARNIも二次性MRの減少に寄与するというものでしたが、MRが比較的軽度なpopulation (mean EROA 0.20 cm2)であり、そのような軽症のレベルでのMRの減少にどこまでの臨床的意義があるかが疑問なのと、高度のMRがある患者群でも同じようにMRが減少できるのかはまだ明らかではありません。
しかし、ARNIがFMRを減少させる機序が興味深いです。両群間で左室容量や僧帽弁のincomplete closure areaに大きな差が見られず、単に左心室のリバースリモデリングを介したMR減少だけでは説明ができなさそうなのです。ARNIによる前・後負荷の変化など血行動態によるものや、弁尖の代償的な成長を促した可能性などが様々挙げられていますが、今後のさらなる解析が待たれます。
その他の心不全治療薬であるSGLT2 inhibitorsやMRAの二次性MR減少に対する効果はまだはっきりしていないようです…。
ARNI以外の報告はいずれもかなり古い研究であり、心不全治療薬の知見が十分広まってきた現在、改めて薬物治療の二次性MRへの影響が評価されています。Moderate-to-severe or Severe MRでGuideline-directed medical therapy (RAAS inhibitors, Beta-blockers, and MRAs)を行ったFMR患者のMRの重症度の変化についての観察研究からの報告です(8)。
MitraClipを検討されたものの、まずは薬物治療を行うことになったLVEF低下を伴う二次性MR患者63名を、ガイドラインに準拠して薬物治療を強化したところ、43名(68%)でGrade 1以上のMR減少が認められました(中央観察期間: 95日)。MRの減少が得られなかった症例の特徴としては、MR減少群と比較して、大きなLV end-diastolic volume、高いEROA/LVEDV比、長いQRS-interval (>120 msec)などの所見が見られました。結果として、36名(57%)はMRが中等度以下まで改善し、カテーテル治療の必要性がなくなっています。
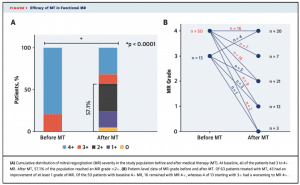
統計学的なlimitationは多いですが、侵襲的治療前に薬物治療を強化することの必要性を改めて示唆する結果だと思います。また、3ヶ月程度で一定のMR減少が得られる、というのもMitraClipなどの治療介入のタイミングの参考になるかもしれません。
また、他の研究でも、薬物治療によるFMRの減少(severe からnon-severe)の予測因子として左脚ブロックが挙げられています(9)。このように左室障害が進行してしまっている症例では薬物治療では十分なMR減少が得られない可能性があることは考慮する必要があるでしょう。
【僧帽弁カテーテル治療における薬物治療】
上述のような二次性MRに対する薬物治療のエビデンスを元に組まれたMitraClipのRCTがCOAPT trialです(1)。RCTの対象患者をコアラボで薬物治療が十分かどうかを含めてスクリーニングし、試験への組み入れの判断を行っています。また、治療後も薬物治療を強化していくというプロトコールになっていました。一方で、そういったプロトコールがなかったのがMITRA-FR trialで、COAPT trialと対照的にMitraClipの優位性を示せなかったRCTです(10)。この2つのRCTの異なる結果の原因を様々な側面から説明が試みられており、薬物治療の内容もその一つの可能性として挙げられています(11)。しかし、これに関しては議論が別れています。上記のようなプロトコールを持っていたCOAPT trialですが、ベースラインの薬物治療の内容はMITRA-FR trialと同程度という結果でした。
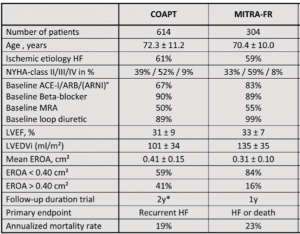
使用用量に関する記載はなく判断できませんが、RAAS inhibitorの導入率に関してはむしろMITRA-FR trialの患者群の方がより高い傾向にありました(67% vs. 83%)。もちろん患者背景の相違もあり、単純なベースラインの薬剤導入率で評価することは難しいです。データで表しにくいですが、患者それぞれの背景に合わせて最大限導入・増量する、ということのほうが大事なのかもしれません。
また、MR治療後に薬物治療を適宜見直していくことも同じように重要だと考えられます。COAPT trialからの報告ではMitraClip治療後の薬剤変更内容も記載されており、治療後に薬剤増量につながった症例が一定数いることがわかります。MRの減少に伴い、血行動態が改善し血圧の上昇などが得られたためと予想されます。別の観察研究では、MitraClip治療後に薬剤の増量ができた症例は予後が良好であることも報告されており(12)、このようにMRの治療後もしっかりと薬物治療を強化できたことが、COAPT trialの結果につながった可能性も考えられます。
【まとめ】
左室収縮能の低下を伴う二次性MRに対する薬物治療は、侵襲的治療介入の前にまず行うべき治療法です。ガイドラインに準拠した適切な薬物治療が二次性MR患者の予後改善につながります。
また、様々な薬剤がMRの減少に寄与することが報告されており、薬物治療のみでMRの減少自体が期待されます。ARNIのPRIME trialでも言及しましたが、その薬物治療によるMRの減少は単に左室のリバースリモデリングだけでは説明ができず、血行動態を含む様々な要素が関与している可能性が示唆されています。しかし、どういった症例でMRの改善が得られにくいかを考慮した上で、次の侵襲的治療介入のタイミングをみつつ、薬物治療をおこなっていくことが必要だと思います。
二次性MRへの侵襲的治療を行う際は、改めてしっかりと薬物治療が強化されていることを確認し、治療後も更に強化の余地がないかチェックすることが重要であると考えられます。
【References】
- Stone GW, Lindenfeld J, Abraham WT, Kar S, Lim DS, Mishell JM, et al. Transcatheter Mitral-Valve Repair in Patients with Heart Failure. N Engl J Med. 2018;379(24):2307-18.
- Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2021.
- Goliasch G, Bartko PE, Pavo N, Neuhold S, Wurm R, Mascherbauer J, et al. Refining the prognostic impact of functional mitral regurgitation in chronic heart failure. Eur Heart J. 2018;39(1):39-46.
- Lowes BD, Gill EA, Abraham WT, Larrain JR, Robertson AD, Bristow MR, et al. Effects of carvedilol on left ventricular mass, chamber geometry, and mitral regurgitation in chronic heart failure. Am J Cardiol. 1999;83(8):1201-5.
- Kotlyar E, Hayward CS, Keogh AM, Feneley M, Macdonald PS. The impact of baseline left ventricular size and mitral regurgitation on reverse left ventricular remodelling in response to carvedilol: size doesn’t matter. Heart. 2004;90(7):800-1.
- Levine AB, Muller C, Levine TB. Effects of high-dose lisinopril-isosorbide dinitrate on severe mitral regurgitation and heart failure remodeling. Am J Cardiol. 1998;82(10):1299-301, A10.
- Kang DH, Park SJ, Shin SH, Hong GR, Lee S, Kim MS, et al. Angiotensin Receptor Neprilysin Inhibitor for Functional Mitral Regurgitation. Circulation. 2019;139(11):1354-65.
- Sannino A, Sudhakaran S, Milligan G, Chowdhury A, Haq A, Szerlip M, et al. Effectiveness of Medical Therapy for Functional Mitral Regurgitation in Heart Failure With Reduced Ejection Fraction. J Am Coll Cardiol. 2020;76(7):883-4.
- Nasser R, Van Assche L, Vorlat A, Vermeulen T, Van Craenenbroeck E, Conraads V, et al. Evolution of Functional Mitral Regurgitation and Prognosis in Medically Managed Heart Failure Patients With Reduced Ejection Fraction. JACC Heart Fail. 2017;5(9):652-9.
- Obadia JF, Messika-Zeitoun D, Leurent G, Iung B, Bonnet G, Piriou N, et al. Percutaneous Repair or Medical Treatment for Secondary Mitral Regurgitation. N Engl J Med. 2018;379(24):2297-306.
- Nishimura RA, Bonow RO. Percutaneous Repair of Secondary Mitral Regurgitation – A Tale of Two Trials. N Engl J Med. 2018;379(24):2374-6.
- Hagnas MJ, Grasso C, Di Salvo ME, Sardone A, Rapisarda P, Pelliccia M, et al. Effect of post-procedural evidence-based therapy on 2-year prognosis after transcatheter mitral valve repair. Eur J Heart Fail. 2021;23(4):677-9.
