結局どうするSecondary MR
早いものでついにreviewも最終回になりました。今回はSHD隆盛の現在も議論が続いている機能性僧帽弁逆流(secondary/functional MR)についてのかなり私見も交え総括的なレビューにしてみました。
[1] 機能性僧帽弁逆流(Secondary MR)はなぜ難しい?
ご存知の通り、MRは一次性(primary)と二次性(secondary)に分類されます。Secondary MRの定義を言葉で表せば、『僧帽弁自体(弁尖と腱索)に異常がなく僧帽弁周囲の組織からの影響により出現するMR』となります。Secondary MRは予後が悪く、severe MRの5年での生存率は30%程度となっています。(文献1)
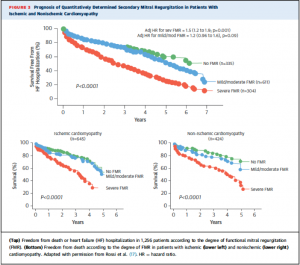 (図1: 文献1より引用)
(図1: 文献1より引用)
下記の図は大変有名なCarpontierによる僧帽弁形態の分類とMRの成因による分類の図ですが、下段がsecondary MRに分類されます。
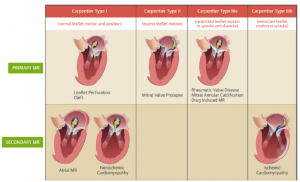 (図2: 文献2より引用)
(図2: 文献2より引用)
図のようにsecondary MRの中でも成因には様々なものがあります。僧帽弁周囲の組織からの影響によるMRは全てsecondaryに分類されるからです。この僧帽弁周囲の組織というやつが曲者で、左心室はもちろんのこと、左心房や僧帽弁輪、SAMによるものまで多様であり、時には並存します。このheterogeneityが我々を悩ませるのです。
私見としては、僧帽弁構造の側面から見ればsecondary MRの大部分は心室由来のsecondary MRと僧帽弁由来のsecondary MR (atrial MR)に分類されると考えています。
心室由来のMRは虚血/心筋症などによる心室拡大から弁輪拡大をきたし、乳頭筋/腱索を介したtentingにより弁尖の接合が妨げられることによって起こります。一方でatrial MRでは僧帽弁のtentingは少なく、心室由来のものとは異なった僧帽弁構造をとります。弁輪拡大に対する弁尖面積が少なく、この不十分な弁尖リモデリングの関与が考えられています。そのほかにも心房機能低下による弁輪収縮不全や弁輪構造変化による弁に対するストレス増大などが考えられています。ちなみに今年改訂された日本循環器学会弁膜症ガイドラインにも心房性機能性MRと表記されています。(文献3)
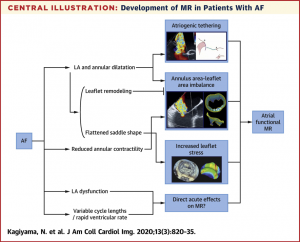 (図3: 文献4より引用)
(図3: 文献4より引用)
ただ現在のところ大規模なRCTなどではsecondary MRは一括りにされて議論されることが多いため、研究の解釈を困難にしている一つの要因と考えています。
[2] 現行のsecondary MRの治療
secondary MRはその名の通り弁そのものの異常ではなく、左室機能不全によるものが多数を占めます。そのため、ガイドラインではMRの治療の前に左室に対する治療(冠動脈血行再建、心不全薬物治療、心室再同期療法など)を考慮するようにrecommendされています。(図4参照)
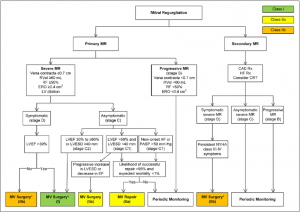 (図4: 文献5より引用)
(図4: 文献5より引用)
一方、近年までsecondary MRにおいて僧帽弁に対するinterventionは良い結果が得られておりませんでした。虚血性MRにおいてMV repairを追加することによる効果をみたrandomized trial (文献6)では、MV 手術によるbenefitは認められませんでした。弁下組織への介入や左室形成術など、様々な手技が検討されているものの、MV手術の有用性は確立されていません。
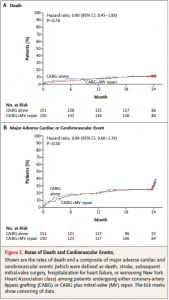 (図5: 文献6より引用)
(図5: 文献6より引用)
しかし昨年secondary MRの治療に大きな革命が起きました。ご存知の方も多いかと思いますがMitraClip®による僧帽弁形成のsecondary MRに対する有効性を示したRCT (COAPT trial)の結果がNEJM誌に発表(文献7)されました。

 (図6: 文献7より引用)
(図6: 文献7より引用)
また、薬剤治療においても心不全治療薬として登場したsacubitril/valsartan vs. valsartan onlyのRCT (PRIME study) (文献8)において、sacubitril/valsartanのsecondary MR抑制効果が示されました。
今後これらのRCTの結果によりガイドラインがどのように改定されるか、注目したいところです。
[3] secondary MRにまつわる議論とその展望
先に述べたCOAPT trial (文献7)はSHD領域のみならず心不全領域においても重要な結果だったのですが、一方時を同じくしてほぼ同様のstudy designで行われたRCT (MITRA-FR trial)(文献9)ではMitraClip®治療による予後の改善効果を認めませんでした。
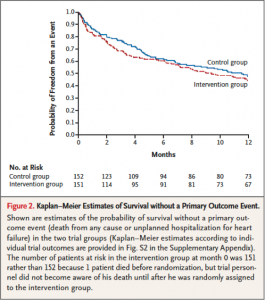 (図7: 文献[9]より引用)
(図7: 文献[9]より引用)
この二つの大規模RCTの異なる結果は同じ号のNEJMに掲載され、結果の解釈について議論がなされました。多くのreviewが既にpublishされているので一つ読んでみると面白いと思います。もっとも有力な説は、左室のダメージとMR重症度の比率の差がが結果に影響を及ぼしたという説です。
両研究の患者背景を比較したところ、MITRA-FRではCOAPTよりも左室のサイズが大きく(indexed LVEDV 135±35 ml/m2 vs 101±34 ml/m2)、MR逆流弁口面積(EROA)は小さい(0.31±10 cm2 vs 0.41±15 cm2)という差が認められました。
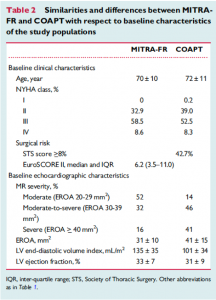 (図8: 文献10参照)
(図8: 文献10参照)
このことから推測された二つのRCTの違いは、左室機能障害の程度とMRの重症度の差であり、左室機能障害に比して僧帽弁逆流症の重症度が高かったCOAPT trialでは良い結果が得られたのではないかと多くの文献で評価されています。次の図をみてください。
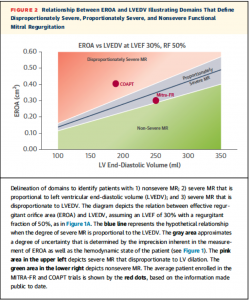 (図9: 文献11より引用)
(図9: 文献11より引用)
このreviewでは、LVEDVをx軸、EROAをy軸とし、青の線を仮想の比例ラインとしてその下(green area)はnon-severe MR, 比例ライン付近(gray area)をproportional severe MR, 比例ラインに比してEROAが高い群をdisproportional severe MRとしています。「Proportional」という言葉は釣り合いの取れた、とかバランスのいい、といった単語なので、それぞれ日本語で言えば均衡性severe MR, 非均衡性severe MRといったところでしょうか。左室障害の度合いと比例せず、MRの度合いが強い症例がMITRA-FRと比してCOAPTに多かったことが一つの要因ではないかとされています。ただこのlogicの問題点はあくまで比例ラインは仮想であり、どの症例が本当にMitraClipによるbenefitを得られるのかはまだ謎のままです。
また、ここで用いられる左室評価はLVEDVが本当に最適なのか、という点も議論の対象となるべきポイントです。とは言えLVEFはMR症例において左室障害を過小評価するのはよく知られています。先日当施設からJACCにpublishされた論文(文献12)では、左室ストレイン(LVGLS: left ventricular global longitudinal strain)を用いた機能性MRの左室機能の評価が予後に関連することを示しました。
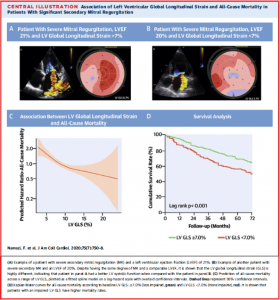 (図10: 文献12より引用)
(図10: 文献12より引用)
今後imaging modalityの発展に伴い評価法も変わっていく可能性がありそうです。しばらくproportional/disproportionalの議論は続きそうですので興味があれば覚えておいて損はないかと思います。
また、僧帽弁自体の構造の及ぼす影響も気になるところです。前述したatrial MRとtethering MRでは僧帽弁形状に明らかに違いがあり、適した治療が異なる可能性があります。さらにCardioband®などの弁輪形成デバイスの有効性も今後注視していくべきかと思います。現在Cardioband®+OMT(optical medical therapy) vs. only OMTとの比較のRCT (ACTIVE trial, NCT03016975)が進行中であり、結果が期待されています。
まとめ:
Secondary MRは予後が悪く、多数の因子が関与する疾患の性質上その治療は複雑である。また、その評価についても現時点では改善すべき点が多く、今後のimaging modalityの発展が期待される。
治療については現時点ではその効果が証明されているものは多くなく、薬物治療、CRTなどのデバイス治療、弁に対するインターベンションなど多側面からのアプローチが必要になると考えられる。
どうすると書いておきながら結論が出ておらず申し訳ありません。ただそれだけまだ研究の余地のある分野であるということです。
今回で私のレビューは最終回です。このレビューを書くことは大変自分の勉強になりました。レビューを読んで、ここが間違ってる! とかここはこういう考えもあるよ! とかツッコミがあればぜひ教えてください。
よろしければ下記アドレスに連絡いただければと思います。
khircvm@gmail.com
K.Hirasawa@lumc.nl
また、今後留学を考えている方からの相談など、なんでもOKです。
最後になりましたが、拙いレビューにお付き合いいただきありがとうございました。また、貴重な機会を与えてくださったSUNRISE lab関係者の皆様に感謝申し上げます。
文献:
[1] Asgar AW, et al. Secondary Mitral Regurgitation in Heart Failure; Pathophysiology, Prognosis, and Therapeutic Considerations J Am Coll Cardiol 2015;65:1231-48.
[2] El Sabbagh, A. et al. Mitral Valve Regurgitation in the Contemporary Era: Insights into Diagnosis, Management, and Future Directions. J Am Coll Cardiol Img. 2018;11(4):628-43.
[3] JCS/JATS/JSVS/JSCS 2020 Guideline on the Management of Valvular Heart Disease.
[4] Kagiyama N, et al. Subtypes of Atrial Functional Mitral Regurgitation; Imaging Insights into Their Mechanisms and Therapeutic Implications. J Am Coll Cardiol Img. 2020;13(3):820-35.
[5] Nishimura RA, et al. 2017 AHA/ACC Focused Update of the 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease. Circulation. 2017;135:e1159–95.
[6] Michler RE, et al. Two-Year Outcomes of Surgical Treatment of Moderate Ischemic Mitral Regurgitation. N Engl J Med 2016;374:1932-41.
[7] Stone GW, et al. Transcatheter Mitral-Valve Repair in Patients with Heart Failure. (COAPT trial) N Engl J Med 2018; 379:2307-18.
[8] Kang DH, et al. Angiotensin Receptor Neprilysin Inhibitor for Functional Mitral Regurgitation. (PRIME Study) Circulation. 2019;139:1354–65.
[9] Obadia JF, et al. Percutaneous Repair or Medical Treatment for Secondary Mitral Regurgitation. (MITRA-FR trial) N Engl J Med. 2018;379:2297-306.
[10] Pibarot P, et al. MITRA-FR vs. COAPT: lessons from two trials with diametrically opposed results. Eur Heart J. 2019;20:620-624.
[11]Grayburn PA et al. Defining “Severe” Secondary Mitral Regurgitation: Emphasizing an Integrated Approach. J Am Coll Cardiol 2014;64:2792–801.
[12]Namazi F et al. Prognostic Value of Left Ventricular Global Longitudinal Strain in Patients with Secondary Mitral Regurgitation. J Am Coll Cardiol 2020;75:750–8.
