TAVI周術期の脳梗塞について
Reviewということで、テーマに沿って論文のレビューなどをさせていただきます。今回は大動脈弁狭窄症に対するTAVIにおける周術期の脳梗塞リスクとそれに対する対策などについてまとめようかと思います。
周術期の脳梗塞はTAVIにおける主要な合併症のうちの一つです。
まず頻度としては、10年前は4-5%ぐらいの頻度でした。PARTNER trialなどの初期のRCTでも同様の頻度でした。また、Real worldのレジストリーデータを見てみると、脳梗塞リスクは徐々に低下傾向で、米国からの最新のデータで30日以内の脳梗塞発症リスクは2%程度です(1)。しかし、治療対象が徐々に低リスク患者へと広がり、周術期死亡率が低下傾向にある中で(30日死亡率: 2012年 7.5% → 2019年 2.5%)、こうした脳梗塞リスクは相対的に低下が乏しい印象で、残念ながらゼロではないというのが現状です。今後TAVIの若年化が進むようであれば、避けなくてはならない合併症のうちの一つでもあると考えられます。大動脈弁狭窄症は治ったけど、麻痺が残ってしまう、などの悲しい結果は避けなくてはなりません。
日本のJTVT registryの最新のデータでは30日以内の脳梗塞発症率は1.3%で、米国と比較するとさらに低めな水準です(JTVT 2019)。
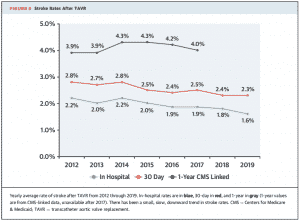
(J Am Coll Cardiol 2020;76:2492–516)
それでは、こうした塞栓症をどのようにすれば防げるのでしょうか。
塞栓症のリスクとしては、手技自体に関するものでいうと大動脈弁バルーン拡張が挙げられています。TAVI中の弁留置前のバルーン拡張を避けることでどれほど塞栓症のリスクを抑えられるかはまだはっきりしていません(2,3)。弁留置後のバルーン拡張が脳梗塞リスクと関係しているとする報告もあります(4)。ただこうしたバルーン拡張が必要な症例の多くは弁の石灰化が強いなどただでさえ脳梗塞のリスクが高そうな患者ばかりですので、こうした背景を十分に加味できているかどうかは議論の余地があります。いずれにせよ、不要なバルーン拡張をなるべく避けるというのは一つの選択肢になりえるかと思います。
患者側のリスク因子としては、腎機能低下やTAVI周術期に新規発症した心房細動などが挙げられていますが(5,6)、いずれも予防的な介入が取りにくいものなので気をつけようがないかと思います。
一方で、周術期の脳梗塞は施設や術者のTAVI症例数と関係なく発症することが知られています(7)。一応、年間200件以上のTAVIを行う術者では脳梗塞発症率が低かったとのことですが、そこまでの症例数をこなす術者は多くないでしょうし、この研究でもnが少なく統計的な妥当性は不透明です。
また、TAVI弁やデリバリーカテーテルも進歩をしていますが、それらの新しいデバイスと古いデバイス間で脳梗塞リスクに有意な差は認められていません(8)。つまり、現在のスタンダードなTAVIの手技を行う中では脳梗塞の発症リスクを抑制することが難しく、交通事故のように一定の確率で起こりえてしまう、ということだと思います。
そのため、塞栓症の予防にはプラスアルファの手技が必要ではないかということで、生まれたのが保護デバイスです。TAVI施行時に飛散する大動脈弁や大動脈壁のデブリや血栓をトラップして塞栓症の発症を予防するというコンセプトです。その中で、Sentinel EPD (Boston Scientific)が欧州および米国での承認を得ていて、臨床での使用が可能となっています。図のように、2つのフィルターがついているカテーテルデバイスとなっていて、右撓骨動脈から進めて左総頸動脈と右腕頭動脈を保護するというものです。
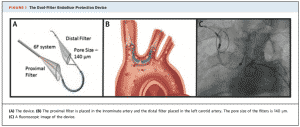
(J Am Coll Cardiol 2017;69:367–77)
2016年に発表されたCLEAN TAVI trial では100名のCorevalve を用いたTF-TAVI 患者を1:1でランダム化して、Sentinel 使用群ではDW-MRIでの新規虚血性病変を44%減少させることを非使用群と比較して有意に少なかったことを示しています(9)。しかし、脳梗塞としてのイベントは両群間では差がみられませんでした。
その後に発表されたSENTINEL trial ではSapienもしくは CorevalveでTF-TAVIを施行した約360名の患者を2:1でSentinel 使用群とコントロール群に割付して、使用効果を検討しています(10)。Sentinel使用の安全性を示すことはできましたが、残念ながらMRIでの虚血性病変や30日の脳梗塞などの臨床イベントに関して優位性を示せませんでした。しかし、一方でSentinel使用群の99%でなんらかのデブリが捕捉されており、多くのTAVI症例でこうした小さな塞栓を原因とする無症候性脳虚血が生じていると考えられます。
少し脱線して別の論文になりますが、こうしたSentinel で捕捉されたデブリの病理学的検討をされています(11)。やはり大動脈弁組織や血栓が多いですが、心筋組織なども塞栓となりうるようです。TAVI弁の種類によってこうしたデブリの成分も異なっていて、面白い結果です。
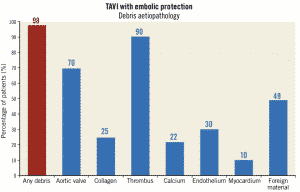
(EuroIntervention 2021;16:1141-1147)
さらに、上述のCLEAN TAVI, SENTINEL trialの2つのRCTとドイツのレジストリーデータであるSENTINEL Ulm registryの患者群を合わせた1,306名の患者における結果も発表されています(12)。結果としては、SENTINEL 使用群でTAVI後72時間以内の脳梗塞に関して65%のrelative risk reduction (1.88% vs. 5.44%)を認めました。
こうしたTAVIにおける脳梗塞に関する研究の難しいところは、もともと発症率が1-2%程度の合併症なのでどうしても統計的にパワー不足になってしまうことであったり、脳梗塞の診断にばらつきがあったり、というところだと思います。脳梗塞の診断については、明らかな麻痺があればわかりますが、神経内科医師なら気づくような微小な機能障害であると患者や循環器内科医師は見落としてしまうかもしれません。そのため、イベントの発症率が論文によって様々となっています。
2021年に発表された最新のTVT Registryからの報告(13)では、かなり多い症例数を用いて保護デバイスの使用効果を検討しています。2018年1月から2019年12月に米国でTAVIを施行したおよそ120,000人のデータで解析しています。観察期間中でSentinelの使用率は経時的に増多傾向であり、2018年第1四半期では全手技の5%でしたが、2019年12月の時点では13%でデバイスが使用されています。しかし、一方で使用頻度については施設間の差も大きく、全599施設のうち72%は全く保護デバイスを使っていないという現状もあります。そして、保護デバイスの使用効果に関しては、Instrumental Variable analysisではデバイスの使用の有無でin-hospital strokeに有意差は認められませんでした。しかし、propensity score match analysisでは、塞栓症予防デバイスの使用がadjusted OR 0.82 [95%CI 0.69-0.97], absolute risk reduction -0.28% [95%CI -0.52 to -0.03]と有意にin-hospital strokeを減少させたという結果でした。
他の観察研究やメタアナリシスのデータをみても、塞栓保護デバイスは一定の使用効果はあると言えると思います。しかし、長期的な医療費についてはまだわからないものの、TAVI入院での治療費がおよそ3,000ドルほど増えてしまなどコストの問題もあるので (14)、保護デバイスの使用に関しては今後適切な患者選択が必要となるかと思います。そのためには、塞栓症のリスクファクターのさらなる評価とそれに基づく保護デバイスの患者選択方法の検討が求められているかと思います。
また、Sentinel以外のデバイスとしてTriGUARD 3 のデータも最近発表されました(15)。大腿動脈から逆行性にカテーテルを進め、弓部大動脈にフィルターをおいて、腕頭動脈・左総頸動脈・左鎖骨下動脈をまとめて保護するというものです。こうしたデバイスの発展も待たれるところです。
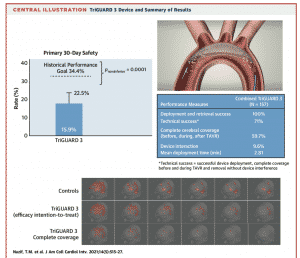
(JACC Cardiovasc Interv 2021;14:515-527)
以上、簡単ではありますが、TAVI周術期の脳梗塞に関する知見についてまとめてみました。なにかご指摘やご意見などあればお気軽にご連絡ください。
ボン大学 リサーチフェロー 田中徹 ta.chi.tsu.tetsu@gmail.com
参考文献
- Carroll JD, Mack MJ, Vemulapalli S et al. STS-ACC TVT Registry of Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2020;76:2492-2516.
- Banerjee K, Kandregula K, Sankaramangalam K et al. Meta-analysis of the Impact of Avoiding Balloon Predilation in Transcatheter Aortic Valve Implantation. Am J Cardiol 2018;122:477-482.
- Leclercq F, Robert P, Akodad M et al. Prior Balloon Valvuloplasty Versus Direct Transcatheter Aortic Valve Replacement: Results From the DIRECTAVI Trial. JACC Cardiovasc Interv 2020;13:594-602.
- Nombela-Franco L, Webb JG, de Jaegere PP et al. Timing, predictive factors, and prognostic value of cerebrovascular events in a large cohort of patients undergoing transcatheter aortic valve implantation. Circulation 2012;126:3041-53.
- Vlastra W, Jimenez-Quevedo P, Tchetche D et al. Predictors, Incidence, and Outcomes of Patients Undergoing Transfemoral Transcatheter Aortic Valve Implantation Complicated by Stroke. Circ Cardiovasc Interv 2019;12:e007546.
- Auffret V, Regueiro A, Del Trigo M et al. Predictors of Early Cerebrovascular Events in Patients With Aortic Stenosis Undergoing Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2016;68:673-84.
- Salemi A, Sedrakyan A, Mao J et al. Individual Operator Experience and Outcomes in Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv 2019;12:90-97.
- Pilgrim T, Lee JKT, O’Sullivan CJ et al. Early versus newer generation devices for transcatheter aortic valve implantation in routine clinical practice: a propensity score matched analysis. Open Heart 2018;5:e000695.
- Haussig S, Mangner N, Dwyer MG et al. Effect of a Cerebral Protection Device on Brain Lesions Following Transcatheter Aortic Valve Implantation in Patients With Severe Aortic Stenosis: The CLEAN-TAVI Randomized Clinical Trial. JAMA 2016;316:592-601.
- Kapadia SR, Kodali S, Makkar R et al. Protection Against Cerebral Embolism During Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2017;69:367-377.
- Kroon H, von der Thusen JH, Ziviello F et al. Heterogeneity of debris captured by cerebral embolic protection filters during TAVI. EuroIntervention 2021;16:1141-1147.
- Seeger J, Kapadia SR, Kodali S et al. Rate of peri-procedural stroke observed with cerebral embolic protection during transcatheter aortic valve replacement: a patient-level propensity-matched analysis. Eur Heart J 2019;40:1334-1340.
- Butala NM, Makkar R, Secemsky EA et al. Cerebral Embolic Protection and Outcomes of Transcatheter Aortic Valve Replacement: Results from the TVT Registry. Circulation 2021.
- Megaly M, Sorajja P, Cavalcante JL et al. Ischemic Stroke With Cerebral Protection System During Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv 2020;13:2149-2155.
- Nazif TM, Moses J, Sharma R et al. Randomized Evaluation of TriGuard 3 Cerebral Embolic Protection After Transcatheter Aortic Valve Replacement: REFLECT II. JACC Cardiovasc Interv 2021;14:515-527.
